Количественные расчеты в химии основываются на нескольких ключевых понятиях: молярная масса, закон Авогадро и массовая доля элемента.
Молярная масса — это масса одного моля вещества. Один моль содержит
![]()
частиц (атомов, молекул и т.д.), что называется числом Авогадро. Молярная масса определяется как отношение массы вещества n в молях:
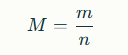
Она измеряется в граммах на моль (г/моль) и численно равна относительной молекулярной массе вещества (сумме атомных масс входящих в его состав элементов). Например, молярная масса воды равна 18 г/моль, что равно сумме масс двух атомов водорода и одного атома кислорода.
Закон Авогадро утверждает: при одинаковой температуре и давлении равные объемы различных газов содержат одинаковое число молекул, равное числу Авогадро, то есть
![]()
частиц. Это позволяет пересчитывать массу газов в объемы и обратно, использовать объемы газов для количественных расчетов.
Массовая доля элемента в сложном веществе показывает, какую часть массы вещества занимает данный элемент. Она вычисляется как отношение массы элемента к массе всего вещества

Массовая доля выражается в долях единицы или процентах. Например, в воде массовая доля водорода примерно 11%, а кислорода — 89%. Сумма массовых долей всех элементов в веществе равна 1 (или 100%).
Таким образом, для количественных расчетов в химии удобно пользоваться молярной массой для перехода между количеством вещества и массой, законом Авогадро для работы с объемами газов и массовой долей для определения состава сложных веществ.
Эти понятия составляют фундамент для химических расчетов и позволяют вычислять массы, объемы и состав веществ в реакциях и смесях.